Перебіг гонартроза і коксартрозу на тлі цукрового діабету
- Вступ Остеоартроз (ОА) страждає кожен п'ятий житель планети [18], причому дане захворювання є найчастішим...
- результати
- Обговорення результатів
- висновки
 Вступ
Вступ
Остеоартроз (ОА) страждає кожен п'ятий житель планети [18], причому дане захворювання є найчастішим серед патології опорно-рухового апарату в різних регіонах земної кулі [11, 17]. ОА несе велику медичну, соціальну та економічну навантаження на суспільство [7], а найбільш актуальною вважається проблема поразок колінних і тазостегнових суглобів, оскільки гонартроз (ГА) і коксартроз (КА) є найбільш инвалидизирующими локалізаціями патологічного процесу [12]. Необхідно відзначити, що число хворих з ГА за 5 років зросла на 42% [9]. Питання діагностики, патогенезу і лікування ГА і КА при супутньої патології вимагають проведення подальших інтенсивних наукових досліджень [6, 14, 19]. Ці проблеми стали ставитися до одних з найбільш актуальних в сучасній ревматології [1].
Добре відомо, що незалежним чинником ризику розвитку ОА є цукровий діабет (ЦД) [2, 5, 13], особливо у хворих з іншими проявами метаболічного синдрому [8]. Було встановлено, що ГА діагностується у 9 з 10 хворих на первинний ОА, при цьому в 13% випадків має місце СД [15]. Колінні суглоби у вигляді дегенеративних змін є основною «точкою докладання» порушень вуглеводного обміну, а з вагою ГА відзначаються прямі кореляційні зв'язки рівня глікемії [4]. Підкреслимо, що ГА зустрічається майже у 30% хворих на ЦД [16], часто поєднуючись з ураженням періартикулярних тканин і хребта [3, 10].
![Підкреслимо, що ГА зустрічається майже у 30% хворих на ЦД [16], часто поєднуючись з ураженням періартикулярних тканин і хребта [3, 10]](/wp-content/uploads/2020/02/uk-perebig-gonartroza-i-koksartrozu-na-tli-cukrovogo-diabetu-2.jpg)
Завданнями даної роботи стали порівняльна оцінка клінічних, рентгенологічних і сонографічних ознак ГА і КА у хворих з різними типами СД і без такого, вивчення зв'язків кістково-деструктивних ознак з порушеннями вуглеводного обміну, в тому числі з фізико-хімічними інтегральними показниками, визначення впливу СД на темпи прогресування змін з боку колінних і тазостегнових суглобів.
Матеріал і методи
Під спостереженням знаходилися 153 хворих ОА, розподілених на дві групи. 1-ю (основну) склали 47 осіб (16 чоловіків і 31 жінка у віці від 25 до 72 років), які страждають ОА на фоні ЦД, а 2-ю (контрольну) - 106 пацієнтів без ЦД (83 чоловіки і 23 жінки у віці від 32 до 73 років). Середній вік в 1-й і 2-й групах відповідно склав 54,0 ± 1,3 і 49,0 ± 0,8 року. Слід підкреслити, що хворі 1-ї групи достовірно відрізнялися від 2-й за статтю та віком. Тривалість ЦД становила 12,0 ± 1,1 року, а вік початку даної ендокринної патології - 42,0 ± 1,9 року. СД типу 1 (СД1) і типу 2 (ЦД2) діагностовано відповідно в 24 і 76% випадків. Параметри середнього артеріального тиску склали 132,0 ± 2,5 мм рт.ст., периферичного судинного опору - 2236,0 ± 64,9 дин 'з' см-5, індексу Кетле - 32,0 ± 0,8 о.е . Вираховували індекс тяжкості ОА (Q) за формулою: {(А + В) 'C' 2}, де А - суглобової рахунок, В - індекс Річі, С - стадія хвороби, 2 - поправочний коефіцієнт для хворих з синовітом, а також підраховували індекси прогресування ГА (R) і КА (S) за формулою: {(С2 + Е): D}, де С - стадія захворювання, Е - сума рентгеносонографіческіх ознак ГА або КА, D - тривалість клінічної маніфестації ГА (КА).
Пацієнтам виконували рентгенологічне (апарат Multix-Compact-Siеmens, Німеччина) та ультразвукове (сонографія Envisor-Philips, Нідерланди) дослідження колінних і тазостегнових суглобів, а також двухенергетіческой рентгенівську остеоденсітометріі проксимального відділу стегнової кістки (денситометр QDR-4500-Delphi-Hologic, США) . У крові вивчали концентрації глюкози, глікозильованого гемоглобіну (HbA1 / c) і інсуліну (аналізатори BS-200; Китай, BIO-RAD-D10, США, PR2100-diagnostic-pasteur, Франція), визначали поверхневий натяг (ПН) сироватки крові, її модуль в'язкоеластичності (ВЕ), кут нахилу (УН) і фазовий кут (ФУ) тензіограм (комп'ютерний Тензіометр ADSA-Toronto, Німеччина - Канада). Вираховували показник інсулінорезистентності HOMA (Homeostatic Model Assessment) за формулою: {(інсулін 'глюкоза): 22,5}, глікемічний коефіцієнт межфазной активності (L) за формулою: {(ПН' інсулін): (глюкоза + HbA1 / c)} і адсорбционно-глікемічний інтегральний коефіцієнт (N) за формулою: {(ПН: ВЕ):: (ФУ: УН) 'глюкоза}.
Статистична обробка отриманих результатів досліджень проведена за допомогою комп'ютерного варіаційного, непараметрического, кореляційного, регресійного, одно- (ANOVA) і багатофакторного (ANOVA / MANOVA) дисперсійного аналізу (програми Microsoft Excel і Statistica-Stat-Soft, США). Оцінювали медіани, їх стандартні відхилення і помилки, коефіцієнти кореляції, критерії регресії, дисперсії, Стьюдента, Уилкоксона - Рао, Макнемара - Фішера і достовірність статистичних показників (р).
результати
У хворих ОА з СД в 3,7 рази частіше в процес залучаються тазостегнові зчленування (p <0,001) і в 1,2 рази - колінні (p = 0,025). Як свідчить ANOVA, СД впливає на тяжкість ГА (р = 0,005) і КА (p <0,001). Ці показники залежать від параметрів N (відповідно р = 0,042 і р = 0,018), але мало пов'язані з L. Встановлено дисперсійне вплив СД на показники Q (р = 0,044), R (р = 0,009) і S (p = 0,027). Крім того, Q прямо корелює зі змістом в крові глюкози (р = 0,011) і HbA1 / c (р = 0,038). Поліартроз встановлений у 98% хворих з СД і у 63% інших (p <0,001), а показники суглобового рахунку відповідно становлять 13,0 ± 1,1 і 6,0 ± 0,5 (p <0,001). Наявність СД значно впливає на інтегральний стан скарг хворих (p = 0,012), що в першу чергу стосується стартовою і ранкової скутості (відповідно р = 0,001 і р = 0,005), а також числа хворобливих суглобів (p <0,001), частота яких у хворих основної групи виявилася відповідно більшою в 1,5 рази (р = 0,038), в 2,2 рази (p <0,001) і в 1,4 рази (p = 0,022). У 55% пацієнтів з СД діагностовано тендовагініти і у 21% ентезопатії, тоді як в контрольній групі - всього лише в 2% (p <0,001) і в 3% (p = 0,003). При цьому частота розвитку реактивного синовіту в обох групах відрізнялася незначно (45 і 54%).
На рис. 1 представлені гістограми показників індексу Лансбурі у хворих ГА і КА з СД і без такого. За даними однофакторного дисперсійного аналізу, СД впливає на індекс Річі (p = 0,007), що відображає тяжкість суглобової патології, а його параметри в 1-й і 2-й групі відповідно становлять 23,00 ± 2,04 і 9,0 ± 0 , 6 (p <0,001). У 81% обстежених хворих виявлено ГА і у 29% - КА, вузлики Гебердена мали місце в 10% випадків, Бушара - в 4%, ознаки спондилоартрозу й остеохондрозу шийного відділу хребта виявлені в 37% спостережень, грудного - у 41%, поперекового - в 63%.
Обговорення результатів
Існує залежність рентгенологічної стадії ОА від наявності СД (p <0,001), середні показники якої в 1,6 рази вище, ніж у 2-й групі (p <0,001). Крім того, супутній ЦД, за даними багатофакторного дисперсійного аналізу Уилкоксона - Рао, впливає на інтегральні рентгеносонографіческіе ознаки уражень колінних суглобів (p <0,001). Однофакторний аналіз демонструє залежність від СД розвитку при ГА остеокистозу (р = 0,020), остеофітоза (р = 0,048), субхондрального склерозу (р = 0,002), епіфізарного остеопорозу (р = 0,036), інтраартікулярних кальцинатов (р = 0,004), лігаментоз (р = 0,007) і хондромних тел (р = 0,42), але не ступеня звуження суглобової щілини, формування кіст Бейкера, тел Гоффа і пелагрі - Штайді. В цілому перераховані статистично значущі складові ГА відповідно виявлені у 30, 55, 64, 38, 18, 16, 13% від числа обстежених хворих.
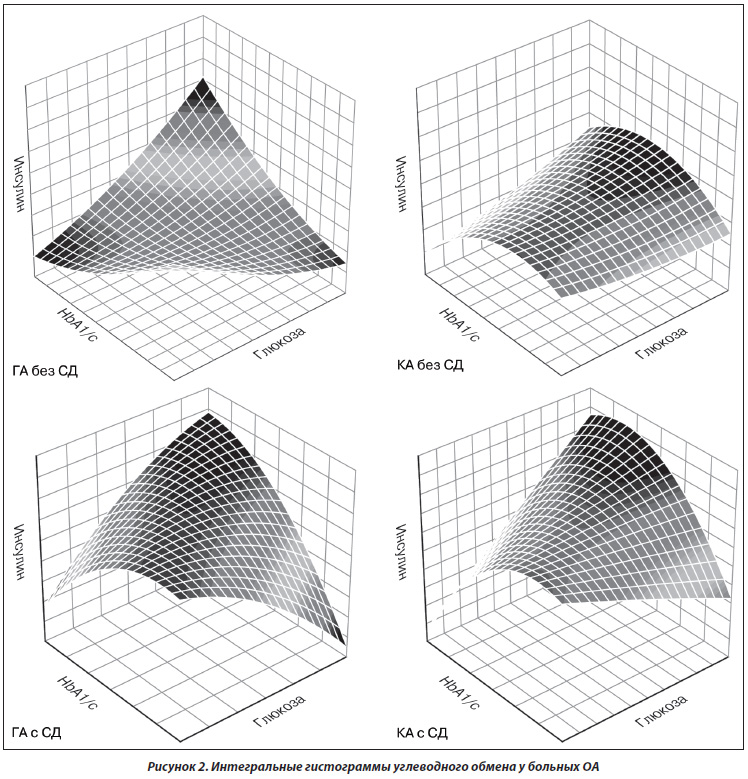
Середній вік хворих на початку маніфестації ГА при СД1 становить 37,00 ± 2,39 року, а при ЦД2 - 50,0 ± 0,9 року (p <0,001). Терміни розвитку ГА і КА після початку СД відповідно становлять 10,00 ± 1,44 і 15,00 ± 2,07 року. В цілому темпи прогресування ГА в групі хворих з СД вище в 2,2 рази (p <0,001), а КА - в 1,8 рази (p <0,001). У порівнянні з СД1 ЦД2 є більш агресивним фактором щодо приєднання КА. На S у хворих ЦД2 впливають показники в крові глюкози (p <0,001), HbA1 / c (p = 0,006), інсуліну (p <0,001), НОМA (p <0,001), L (p = 0,045) і N (p = 0,023), а при СД1 - тільки глюкози (p = 0,002) і HbA1 / c (p = 0,017). На рис. 2 знайшли своє відображення інтегральні гістограми основних параметрів вуглеводного обміну у хворих на ГА і КА.
За даними ANOVA / MANOVA, тип СД мало впливає на характер скарг хворих ОА з боку як колінних, так і тазостегнових зчленувань, але у хворих ГА визначає припухлість суглобів (p = 0,038), яка в 4,5 рази частіше спостерігається при ЦД2 (p = 0,036). Крім того, в цій підгрупі пацієнтів в 1,4 рази частіше реєструється стартова і ранкова скутість (p = 0,003), але в 2,5 рази рідше виникають тендовагініти (p = 0,004) і в 21,8 рази - ентезопатії (p <0,001 ). Останні два клінічнихознаки захворювання фактично відрізняють ГА при СД1 і ЦД2. Слід зазначити, що сумарний індекс Річі у хворих ГА з СД1 і ЦД2 між собою відрізняється несуттєво, відповідно складаючи 18,00 ± 3,04 і 17,00 ± 1,15.
Існує вплив типу СД на локалізацію ОА (p <0,001). Зауважимо, що при ЦД2 в 3,1 рази частіше діагностується КА (p = 0,009) і в 1,5 рази - ГА (p = 0,003). Тип СД надає виразне вплив на тяжкість ураження колінних суглобів (p = 0,011). Розвиток вузликів Гебердена і Бушара при ГА і КА спостерігається виключно у випадках ЦД2, а частота і локалізація спондилопатии у хворих СД1 і ЦД2 приблизно дорівнює. Від типу СД не залежить і поширеність ураження хребта.
Мають місце велика вираженість рентгеносонографіческіх ознак ГА при ЦД2 (p = 0,013) і вплив типу СД на ці інтегральні показники (p = 0,008). Від типу СД залежить частота остеокистозу (p = 0,029), субхондрального склерозу (p = 0,004), лігаментоз (p = 0,015), хондромних тел (р = 0,040) і кіст Бейкера (р = 0,048). Тяжкість перебігу ГА превалює у хворих ЦД2, хоча виникнення тендовагінітів, ентезопатій і лігаментоз є переважно долею пацієнтів з СД1. Регресійний аналіз показує зворотну залежність від клінічних ознак СД вираженості синовіту колінних суглобів (p = 0,042). Існує вплив тяжкості діабетичної макро- і мікроангіопатії на запалення суглобової мембрани (p = 0,028) і ступінь вираженості болю в колінних зчленуваннях (р = 0,042).
Необхідно відзначити, що показники HbA1 / c і L впливають на тяжкість у хворих ГА і КА ентезопатій (відповідно p = 0,026 і р = 0,047) і спондилопатии (p = 0,041 і р = 0,033), а инсулинемии і N - на вираженість синовіту (p = 0,017 і р = 0,007), тендовагінітів (p = 0,019 і р = 0,046), ентезопатій (p <0,001 і р = 0,008). Має місце зворотна регрессионная залежність спондилопатии від концентрації в крові пацієнтів з ГА і КА HbA1 / c (p = 0,049), тендовагінітів і ентезопатій - від вмісту інсуліну (відповідно p = 0,023 і p = 0,014). Крім сказаного, рівень инсулинемии прямо асоціюється з тяжкістю перебігу ГА (р = 0,006) і КА (р = 0,016).
висновки
1. СД у хворих ОА визначає число уражених суглобів у вигляді поліартрози, не тільки стартову, а й ранкову скутість, збільшення частоти окремих рентгеносонографіческіх ознак суглобового синдрому, тяжкість залучення в процес хребта, колінних і тазостегнових зчленувань, що залежить від показників инсулинемии і HbA1 / з в крові.
2. Розвиток ГА і КА частіше спостерігається при ЦД2, який є більш агресивним фактором щодо ураження тазостегнових суглобів, тоді як переважно СД1 у хворих ГА викликає поява тендовагінітів і ентезопатій, а вираженість синовіту в таких випадках пов'язана з діабетичної макро- і микроангиопатией.
3. Наявність СД у пацієнтів з ГА впливає на формування остеокистозу, остеофітоза, субхондрального склерозу, остеопорозу, інтраартікулярних кальцинатов, лігаментоз і внутрішньосуглобових хондромних тел.
4. В майбутньому буде корисним у хворих на ЦД активну раннє виявлення ГА і КА для подальших своєчасних реабілітаційних заходів, а виявлення порушень вуглеводного обміну при такій суглобової патології може мати практичну значимість як фактора ризику окремих структурних змін з боку артикулярних і періартикулярних тканин.
Список літератури
1. Allen KD Patient and provider interventions for managing osteoarthritis in primary care: Protocols for two randomized controlled trials / KD Allen, HB Bosworth, DS Brock, JG Chapman // BMC Musculoskelet. Disord. - 2012. - Vol. 13, № 1. - P. 6065.
2. Berenbaum F. Diabetesinduced osteoarthritis: from a new paradigm to a new phenotype / F. Berenbaum // Ann. Rheum. Dis. - 2011. - Vol. 70, № 8. - P. 13541356.
3. Burner TW Diabetes and rheumatic diseases / TW Burner, AK Rosenthal // Curr. Opin. Rheumatol. - 2009. - Vol. 21, № 1. - P. 5054.
4. DaviesTuck ML Increased fasting serum glucose concentration is associated with adverse knee structural changes in adults with no knee symptoms and diabetes / ML DaviesTuck, Y. Wang, AE Wluka [et al.] // Maturitas. - 2012. - Vol. 72, № 4. - P. 373 378.
5. Ernst K. Keeping active with diabetes and arthritis / K. Ernst, MA Minor // Diabetes Self. Manag. - 2009. - Vol. 26, № 3. - P. 3642.
6. Gelber AC Knee pain and osteoarthritis: lessons learned and lessons to be learned / AC Gelber // Ann. Intern. Med. - 2011. - Vol. 155, № 11. - P. 786 787.
7. HarrisHayes M. Relationship of acetabular dysplasia and femoroacetabular impingement to hip osteoarthritis: a focused review / M. HarrisHayes, NK Royer // PMR. - 2011. - Vol. 3, № 11. - P. 10551067.
8. Inoue R. Medical problems and risk factors of metabolic syndrome among radiographic knee osteoarthritis patients in the Japanese general population / R. Inoue, Y. Ishibashi, E. Tsuda [et al.] // J. Orthop. Sci. - 2011. - Vol. 16, № 6. - P. 704 709.
9. Jämsen E. Primary knee replacement for primary osteoarthritis in the aged: gender differences in epidemiology and preoperative clinical state / E. Jämsen, P. Jäntti, T. Puolakka, A. Eskelinen // Aging. Clin. Exp. Res. - 2012. - Vol. 10, № 9. - P. 135 137.
10. Mader R. Diabetes mellitus and hypertension as risk factors for early diffuse idiopathic skeletal hyperostosis (DISH) / R. Mader, I. Lavi // Osteoarthritis Cartilage. - 2009. - Vol. 17, № 6. - P. 825 828.
11. Marhadour T. Osteoarthritis epidemiology and risk factors / T. Marhadour, D. Guellec, A. Saraux [et al.] // Soins. - 2012. - Vol. 768, № 9. - P. 2829.
12. Michon F. Osteoarthritis. A public health problem / F. Michon // Soins. - 2012. - Vol. 768, № 9. - P. 2728.
13. Nielen MM Cardiovascular disease prevalence in patients with inflammatory arthritis, diabetes mellitus and osteoarthritis: a crosssectional study in primary care / MM Nielen, AM van Sijl, MJ Peters [et al.] // BMC Musculoskelet Disord. - 2012. - Vol. 21, № 13. - P. 150 155.
14. Pereira D. The effect of osteoarthritis definition on prevalence and incidence estimates: a systematic review / D. Pereira, B. Peleteiro, J. Araújo, J. Branco // Osteoarthritis Cartilage. - 2011. - Vol. 19, № 11. - P. 12701285.
15. Racaza GZ Clinical profile of Filipino patients with osteoarthritis seen at two arthritis clinics / GZ Racaza, EO Salido, EG Penserga // Int. J. Rheum. Dis. - 2012. - Vol. 15, № 4. - P. 399 406.
16. Ray S. Prevalence of rheumatic conditions in patients with diabetes mellitus in a tertiary care hospital / S. Ray, AR Datta, P. Sinhamahapatra [et al.] // J. Indian Med. Assoc. - 2011. - Vol. 109, № 2. - P. 7478.
17. Tangtrakulwanich B. Epidemiology and risk factors of patellofemoral osteoarthritis in adults: a populationbased study in southern Thailand / B. Tangtrakulwanich, P. Suwanno // J. Med. Assoc. Thai. - 2012. - Vol. 95, № 8. - P. 10481052.
18. Wang M. Recent progress in understanding molecular mechanisms of cartilage degeneration during osteoarthritis / M. Wang, J. Shen, H. Jin, HJ Im. // Ann. NY Acad. Sci. - 2011. - Vol. 1240, № 12. - P. 6169.
19. Zhai Y. Basic research progress of knee osteoarthritis / Y. Zhai, GD Gao, SY Xu // Zhongguo Gu Shang. - 2012. - Vol. 25, № 1. - P. 8387.